Is het i.p.v. B12-tekort misschien
Methylene-THF-Reductase deficiëntie?


| Door Paula Bailly | Najaar 2013 |
|
Om de zaak wat te vereenvoudigen wil ik de oorzaken voor B12-tekort
opdelen in twee categorieën: Hoewel er over de te weinig opname van B12 al het nodige geschreven is
wil ik toch nog even kort herhalen hoe dat ook al weer zit,
zodat ook de verschillen met de teveel uitscheiding van B12 duidelijk kunnen worden. |

|
|
De oorzaken van te weinig B12 opname liggen in het maag-darmkanaal: De oplossing is relatief simpel: B12-suppletie buiten het maag-darmkanaal om.
Er zijn twee manieren om te zorgen dat de B12 direct in de bloedbaan komt: Om te weten wat de invloed van deze vorm van B12-tekort is moeten we de Foliumzuur-cyclus wat beter bekijken. De Foliumzuur-cyclus is de cyclus waarbij THF (in een paar stappen) in methyl-THF wordt omgezet (plaatje hieronder). Let op: nadat het methyl-THF zijn methyl-groep heeft afgegeven aan Cobalamine, is het weer THF geworden en kan de cyclus opnieuw beginnen. 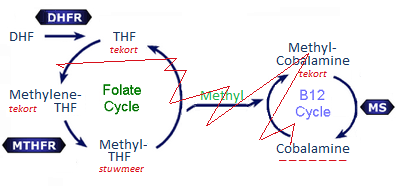
Wat gebeurt er nu als er een Cobalamine (B12) tekort is? Door naar bovenstaand plaatje te kijken kunnen we beredeneren wat er gebeurt: veel van de methyl-THF zal zijn methyl-groep niet kwijt kunnen. |
Waarom zit er geen IF in vitamine B-complex supplementen? Intrinsic Factor wordt in de maagwand afgescheiden en bindt zich vervolgens in de twaalfvingerige darm aan Cobalamine. Daarna kan de Cobalamine in de dunne darm opgenomen worden door het lichaam. Het lijkt zo logisch: als intrinsic factor (IF) zo ontzettend nodig is om B12 op te kunnen nemen in het maag-darmkanaal, dan stop je dat toch gewoon ook in vitamine-supplementen? Het heeft er wel in gezeten: zelf had ik nog een doosje Dagravit B-complex liggen, gefabriceerd in 2011, dat het nog wel bevat. Nu (in 2013) heb ik bij de drogist alle vitamine-supplement-doosjes bekeken: nergens zit het meer in. IF wordt gewonnen uit de magen van koeien en varkens. Het bleek dat mensen hier soms antistoffen tegen aanmaken. Deze antistoffen leiden weer tot -soms heftige- maagkrampen. |
|
Hoe weten we nu of we te maken hebben met een B12-tekort door te weinig opname (of heropname of verhoogd verbruik), of dat we te maken hebben met B12-tekort door te veel uischeiding (laag B12-niveau)? Het methyleren en demethyleren van Cobalamine gebeurt in het waterige gedeelte van de cellen. In het waterige gedeelte (cytosol) drijven ook de mitochondriën, de energie fabriekjes van de cel. In de mitochondriën is ook een lopende band van Cobalamine aan het werk. Alleen vervoert die geen methyl, maar adenosyl. (De scheikundige naam van adenosyl is 5-deoxy-adenosine). Als er in het cytosol nu ècht te weinig Cobalamine is voor de methyl lopende band, (dus niet dat er alleen een door het lichaam geregeld laag niveau is), dan mogen ze wel wat Cobalamine lenen van hun buren: de mitochondriën. Alleen ontstaat er in de mitochondriën nu ook een B12-tekort! De adenosyl lopende band in de mitochondriën werkt dan niet meer goed. Dit heeft tot resultaat dat er een afvalproduct onstaat: Methyl-Malonic-Acid (MMA). De verhoogde aanwezigheid van deze afvalstof kan gemeten worden. In de reguliere geneeskunst is het dan ook gebruikelijk om een B12-tekort op te sporen door met laboratoriumtesten te checken of het Methyl-Malonic-Acid niveau verhoogd is. Is het Methyl-Malonic-Acid niveau niet verhoogd, maar is er toch een laag B12 niveau? B12-tekort door Overmatige uitscheiding van B12 wordt veroorzaakt
doordat er te weinig methyl-THF in het lichaam circuleert.
Er moet dus gekeken worden naar wat daar de oorzaak van zou kunnen zijn: Het is onverstandig om gelijk maar zondermeer Foliumzuur te supplementeren. Foliumzuur wordt namelijk bij lagere doses al schadelijk wanneer er te weinig Methylene-THF-Reductase is. (zie kader 'Wanneer wordt gesupplementeerd Foliumzuur schadelijk?') Naar Deel 3In het voorgaande is uitgelegd dat er naast B12-tekort door te weinig opname nog een andere vorm van B12-tekort is: B12-tekort door te veel uitscheiding. Deze laatste vorm blijkt een nauwe samenhang te hebben met deficiëntie van het enzym Methylene-THF-Reductase (MTHFR deficiency). In Deel 3 wordt verder ingegaan op MTHFR deficiency. |
Hoe ontstaat MMA? In de mitochondriën van de cellen wordt energie gegenereerd via de Citroenzuur-Cyclus (Krebs Cycle). De hoofd-brandstof is Glucose (uit koolhydraten), dat via een aantal stappen wordt omgezet tot iets bruikbaars om energie van te maken: Acetyl-CoA.
(brandstof)
Glucose
|
`.-> Acetyl-CoA
|
v
.--------.
^ \
.---| |
/ | v
| `Succinyl<-' <-.
| -CoA ^
v |
ENERGIE extra
brandstof
(Methyl-Malonyl-CoA)
Om deze energie cyclus wat meer te ondersteunen is er,
behalve Glucose, ook nog wat andere toevoer
van energierijke stoffen mogelijk:
enkele amimozuren en ook nog een klein beetje Homocysteďne.
Deze stoffen worden eerst omgezet in Methyl-Malonyl-CoA. En dit Methyl-Malonyl-CoA kan dan weer worden omgezet in een voor de Citroenzuur-Cyclus bruikbare stof: Succinyl-CoA. Voor deze laatste stap is weer een enzym nodig (Methyl-Malonyl-CoA Mutase).
Maar dit enzym werkt alleen goed met Adenosyl-Cobalamine als co-enzym! | |
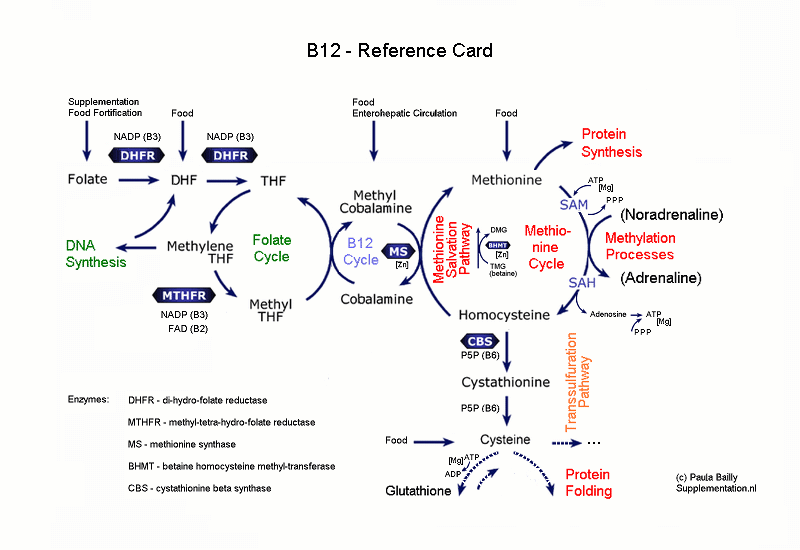
| ||